重组蛋白糖基化鉴定:新靶点的探索与细胞功能关联分析
- 北京百泰派克生物科技有限公司2023年10月16日 1:59 点击:167
糖基化是一种重要的蛋白质修饰方式,它在细胞信号传导、蛋白质稳定性和功能调控等方面起着关键作用。研究人员通过对重组蛋白糖基化的鉴定,可以探索新的靶点,并进一步分析这些靶点与细胞功能的关联。本文将介绍重组蛋白糖基化鉴定的原理和方法,并探讨其在新靶点探索和细胞功能关联分析中的应用。
一、重组蛋白糖基化鉴定的原理
糖基化是指糖分子与蛋白质分子之间的共价结合。在细胞中,糖基化通常发生在蛋白质的氨基酸残基上,如谷氨酸、天冬氨酸和赖氨酸等。糖基化的类型多种多样,包括N-糖基化、O-糖基化和糖脂基化等。
重组蛋白糖基化鉴定是通过一系列实验技术和分析方法,确定蛋白质上是否存在糖基化修饰,并进一步鉴定糖基化的类型和位置。这种鉴定方法主要基于质谱技术,包括质谱分析和质谱成像等。
二、重组蛋白糖基化鉴定的方法
1. 质谱分析
质谱分析是重组蛋白糖基化鉴定的主要方法之一。它通过将待测蛋白质进行酶解,得到糖基化肽段,并利用质谱仪进行分析。质谱分析可以确定糖基化的类型和位置,同时还可以定量分析糖基化的程度。
2. 质谱成像
质谱成像是一种新兴的重组蛋白糖基化鉴定方法。它将质谱分析与组织切片相结合,可以在组织层面上进行糖基化的空间分布分析。质谱成像可以提供更加直观的信息,帮助研究人员了解糖基化在细胞和组织中的分布情况。
三、重组蛋白糖基化鉴定的应用
1. 新靶点的探索
重组蛋白糖基化鉴定可以帮助研究人员探索新的糖基化靶点。通过分析糖基化修饰的蛋白质,可以发现一些以前未知的糖基化靶点,并进一步研究它们在细胞功能调控中的作用。这为新药物的研发和治疗靶点的选择提供了重要的依据。
2. 细胞功能关联分析
重组蛋白糖基化鉴定还可以帮助研究人员分析糖基化与细胞功能的关联。通过对糖基化修饰的蛋白质进行功能研究,可以揭示糖基化在细胞信号传导、蛋白质稳定性和功能调控等方面的作用机制。这有助于深入理解细胞的生理和病理过程,并为疾病的治疗提供新的思路。
重组蛋白糖基化鉴定是一种重要的研究方法,可以帮助研究人员探索新的糖基化靶点,并进一步分析糖基化与细胞功能的关联。随着技术的不断发展,重组蛋白糖基化鉴定在生物药物领域的应用前景将更加广阔。我们相信,通过对重组蛋白糖基化的深入研究,将为新药物的研发和疾病的治疗带来新的突破。
四、重组蛋白糖基化鉴定在新靶点探索中的应用
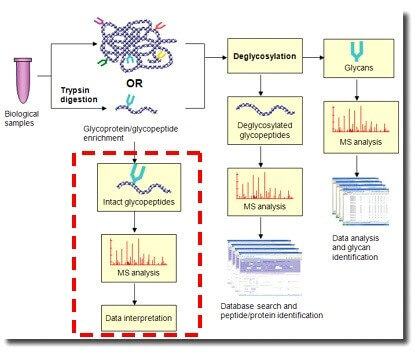
图1
重组蛋白糖基化鉴定在新靶点探索中具有重要的应用价值。通过对糖基化修饰的蛋白质进行鉴定和分析,可以发现与疾病相关的糖基化靶点,并进一步研究其在疾病发生和发展中的作用机制,为疾病的治疗提供新的靶点和策略。
例如,在肿瘤研究中,重组蛋白糖基化鉴定已经被广泛应用。通过对肿瘤细胞中糖基化修饰的蛋白质进行鉴定和分析,有利于发现与肿瘤发生和发展相关的糖基化靶点,并进一步研究其在肿瘤细胞增殖、转移和耐药等方面的作用机制。这些研究为肿瘤治疗提供了新的靶点和策略,例如针对糖基化修饰的蛋白质开发的新型抗肿瘤药物。
此外,重组蛋白糖基化鉴定还可以用于研究神经退行性疾病等神经系统疾病。通过对糖基化修饰的蛋白质进行鉴定和分析,可以发现与神经系统疾病相关的糖基化靶点,并进一步研究其在疾病发生和发展中的作用机制,为疾病的治疗提供新的靶点和策略。
联系我们
| 点击立即咨询>> | 点击提交需求>> |
| 科研服务电话:182-4221-8588 | 访问品牌官网>> |
百泰派克生物科技-生物药物表征,生物质谱多组学优质服务商
北京百泰派克生物科技有限公司(Beijing Bio-Tech Pack Technology Company Ltd. 简称BTP)从事以生物质谱为依托的生物药物表征,大分子物质(包括蛋白质、多肽、代谢物)质谱分析以及小分子物质检测服务。
1、公司采用ISO9001质量控制体系,专业提供以质谱为基础的CRO检测分析服务;
2、获国家CNAS实验室认可,为客户提供符合全球药政法规的药物质量研究服务;
3、业务范围覆盖蛋白质组学、多肽组学、代谢组学、生物药物表征、单细胞分析、单细胞质谱流式、生信云分析以及多组学生物质谱整合分析等;
4、7大质量控制检测平台,满足您一站式服务需求;
5、服务3000+企业,10000+客户的选择;
6、致力于为您提供优质的生物质谱分析服务!

联系邮箱:kefu@labbase.net
版权与免责声明
- 凡本网注明“来源:来宝网”的所有作品,版权均属于来宝网,转载请必须注明来宝网, //www.next-search.com,违反者本网将追究相关法律责任。
- 本网转载并注明自其它来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
- 如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。