信号素3A 在正畸牙齿移动中的潜在作用
- 上海泉众机电科技有限公司2024年1月28日 10:46 点击:151
因治疗需要而出现牙齿和下颌错位的发生率很高。近年来,正畸牙齿移动矫正牙齿错位的生物学研究日益重要,总体目标是确定通过施加力激活的分子因子。在正畸牙齿移动过程中,正畸力的作用导致牙槽骨的机械变化。尽管每个解剖位置的骨细胞(包括成骨细胞、破骨细胞和骨细胞)都对机械负荷敏感,从而适应改变的外部条件,但现在人们认识到,对于正畸牙齿移动,作用在牙周膜(PDL)和内部成纤维细胞上的力是决定性的。然而,力接收和随后的机械转导的确切模式尚不完全清楚,该过程中涉及的分子因子也尚未被鉴定和进行功能表征。
到目前为止,Ephrin/Eph受体家族的成员以及信号素(Semaphorins)及其受体神经纤毛蛋白(Neuropilin)和神经丛蛋白(Plexin)与维持骨稳态有关。研究已经证实了Ephrines 和Eph受体参与正畸牙齿移动过程中的骨重塑,但尚未证明信号素在正畸牙齿移动过程中的参与。然而,信号素3A(Sema3A)对这一作用特别感兴趣,因为它同时诱导成骨细胞分化并干扰破骨细胞分化。研究表明,Nrp1是成骨细胞和破骨细胞Sema3A-依赖性调控的决定性共受体,然而,实际的信号传递是通过 Plexin-A1 受体(PlxnA1)进行的。关于Sema3A机械调控的数据很少。
德国海德堡大学口腔正畸和口腔颌面骨科的Sinan Şen、Christopher J Lux和Ralf Erber研究员在之前的研究中对 Ephrin/Eph 家族成员的研究以及Sema3A 在骨重塑的中的功能数据表明,神经引导分子在正畸牙齿移动调控中的作用可能被低估了。因此,在之后的一项研究中旨在(i)研究不同的机械力是否调节牙槽骨牙周成纤维细胞和成骨细胞中 Sema3A 及其受体 Neuropilin-1 和 Plexin A1 的表达,(ii)研究 Sema3A 的机械调控,(iii)研究 Sema3A 刺激对牙槽骨成骨细胞分化的影响,(iv)阐明 Sema3A-依赖性成骨细胞分化的潜在分子机制,最后(v)测试 Sema3A 对牙槽骨成骨细胞粘附和运动的潜在影响。具体内容发表在 International Journal of Molecular Sciences 期刊题为“A Potential Role of Semaphorin 3A during Orthodontic Tooth Movement”。

表明Sema3A参与调控正畸牙齿移动期间骨重塑的决定性先决条件是它通过牙周组织细胞(人牙周膜原代成纤维细胞(hPDLF)和人牙槽骨原代成骨细胞(hOB)中的机械力进行调节。因此,实验首先研究了hPDLF 和 hOB 中 Sema3A 表达及其受体 NRP1和PLXNA1的机械调控。
在施加机械静态应变(2%、4、24、48、72和96 h)或静态压缩力( 30 g/cm²,1、6、10 h)后,通过定量PCR检测hPDLF细胞的变化。结果表明,在PDLF中,Sema3A的表达明显改变,应变或压缩力作用下的差异调控也明显变化。Sema3A在应变4h和72h后被显著诱导,在96h后达到基线水平,而压缩力导致Sema3A mRNA在所有时间点的表达显著降低。PLXNA1仅在应变4h后被显著诱导,并在24h后升高,而在压缩后没有显著改变。NRP1 在应变4 h后被轻微诱导,但在48h后显著降低,并在应变 72h和 96h和压缩力后仍低于基线水平(图1 A-C)。
Western blot 的蛋白表达分析证实了Sema3A的应变依赖性诱导,并提示了差异调节的受体表达:应变诱导bot、Plexin A1和Neuropilin 1表达,但通过压缩降低。此外,Sema3A蛋白表达被压缩降低,PlexinA1 和 Neuropilin 1 的mRNA 和蛋白质表达在应变及压缩期间表达不一致,Sema3A的mRNA和蛋白表达在时间上也存在差异。
有趣的是,在hOB中施加机械力后,没有观察到Sema3A及其受体表达的显著变化。
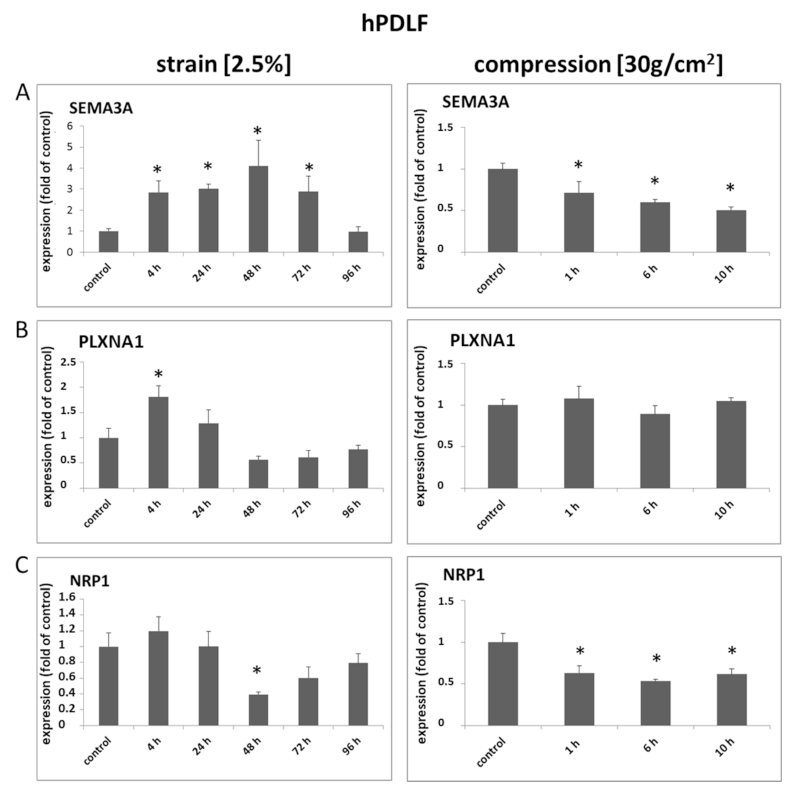
图1 SEMA3A、PLXNA1 和 NRP1 的 mRNA 表达受到机械压缩或应变的差异调节。
基于现有证据表明 Sema3A 可能是 Osterix(SP7)转录因子的直接转录靶点以及来自正畸牙齿移动动物模型的数据显示 Osterix 可以在张力侧被诱导,因此,实验推测应变、Osterix 和 Sema3A 表达可能与 hPDLF 相关。在机械应变(2.5%)或压缩力(30 g/cm²)下对 hPDLF 中 Osterix 进行 RT-qPCR 分析,结果显示,在拉伸细胞中显著诱导Osterix表达长达24h,而压缩hPDLF中Osterix表达显著降低。尽管导致其机械诱导的机制尚不清楚,但这些结果表明,Osterix可能参与了机械诱导的Sema3A上调。
接下来,为了测试Sema3A对牙槽骨成骨细胞成骨分化的影响,用含有或不含重组人Semaphorin 3A 的成骨培养基(10 ng/mL)刺激hOB。
结果显示,外源性Sema3A显著刺激关键成骨转录因子RUNX2表达,其他成骨标志基因(ALPL、碱性磷酸酶、SPP1、骨桥蛋白、BGLAP、骨钙素)在刺激后显示出超越成骨培养基作用的诱导趋势(图2 A-D)。然而,在没有成骨预处理的情况下,Sema3A对成骨基因表达的影响是无法检测到的。因此,PDLF 中Sema3A 的机械-依赖性释放可能仅在已经成骨的环境中促成牙槽骨成骨细胞的成骨分化。
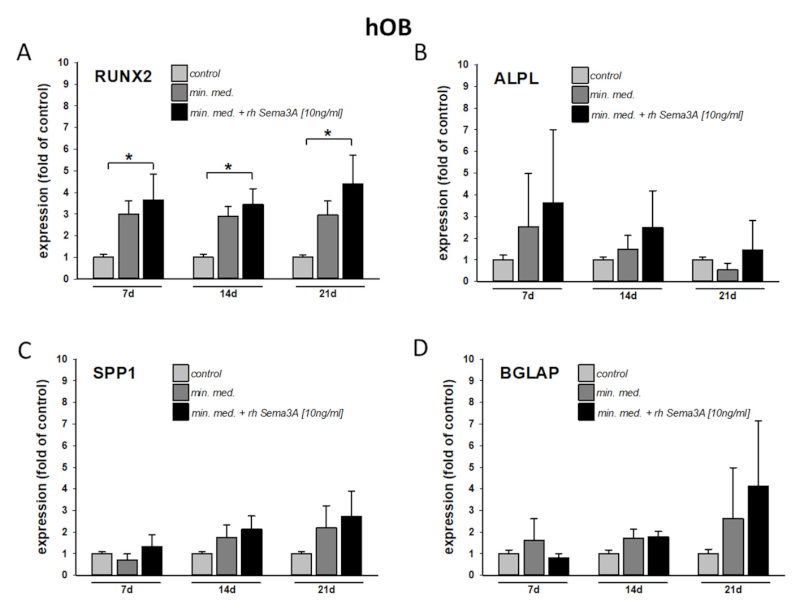
图2 在成骨环境下,外源性信号蛋白3A刺激有助于牙槽骨成骨细胞的成骨分化。
来自小鼠实验的数据表明,丛蛋白相关 GTPases 和 Wnt/β-catenin 信号通路参与骨骼中 Sema3A 激活的信号转导。因此,研究人员测试了 hOB 中 Sema3A 刺激是否导致 GTPases Rac1 的激活和积累以及β-catenin 的核易位。用外源性Sema3A刺激牙槽骨成骨细胞导致Rac1GTPase的激活(图3 A)。
RT q-PCR显示,在矿化培养基中生长的hOB中,Sema3A对β-catenin 诱导有显著贡献(图3 B)。在对照细胞中,β-catenin 主要存在于细胞质中,用 Sema3A 刺激导致 2h后核周 β-catenin 的积累,48h后,大部分β-catenin 易位到细胞核中(图3 C)。基于这些结果,可以推测 hOB 中 Sema3A-依赖性诱导的成骨标志物基因的表达是通过Rac1GTPase- 和β-catenin- 依赖性信号通路发生的。
在几种细胞类型中,Sema3A在与Neuropilin-1 及其共受体PlexinA1结合时激活信号转导级联反应,从而控制F-肌动蛋白动力学,控制细胞粘附和运动。在骨重塑过程中,成骨细胞前体和成骨细胞募集到活跃的重塑部位需要这些细胞的运动。最后,为了检测 Sema3A是否影响牙槽骨成骨细胞运动,用重组 Sema3A(100 ng/mL)处理不同时间段的 hOB,用免疫荧光染色法测定黏着斑蛋白(Vinculin)来评估黏着斑,结果显示,没有证据表明牙槽骨成骨细胞的黏着斑改变。从这些数据来看,Sema3A似乎对牙槽骨中成骨细胞运动没有显著影响。
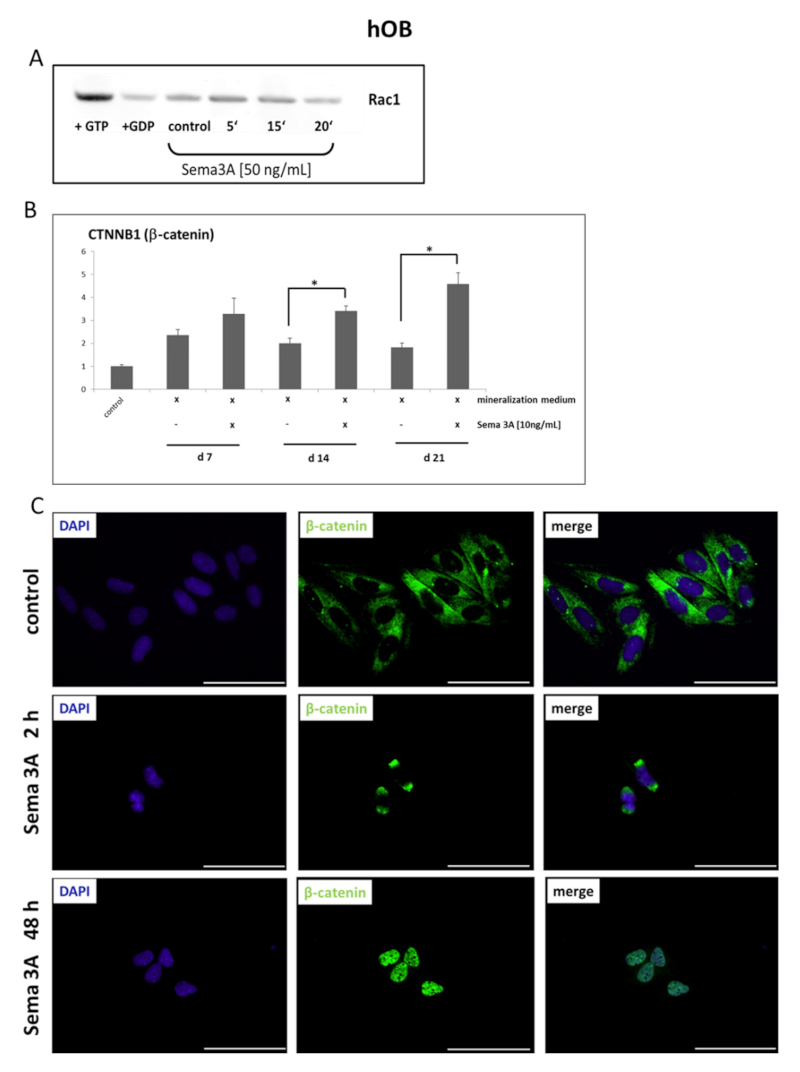
图3 Semaphorin 3A刺激人牙槽骨原代成骨细胞(hOB)与Rac1GTPase激活、β-catenin转录诱导和核易位相关。
以前的研究尚不清楚机械力可能对Sema3A信号传导产生什么影响。总之,这项研究首次显示了牙周成纤维细胞中Sema3A的差异机械调节机制。牙槽骨成骨细胞通过 Rac1 和 β-catenin 依赖性诱导分化标志物对 Sema3A 刺激做出反应。结合之前对 Ephrin/Eph 家族的研究结果,目前的数据表明,神经引导分子参与了正畸牙齿移动过程中骨重塑的调节。Sema3A 信号转导的机械调节可能不一定局限于正畸牙齿移动期间的骨重塑,因为用于维持骨量的基本重塑过程是机械诱导的骨骼范围。然而,在正畸力诱导的骨重塑的情况下,根据这里提供的结果,牙周成纤维细胞作为机械力的受力者,似乎是最重要的。这些体外研究结果能否用于临床,目前还在探索之中。
参考文献:Şen S, Lux CJ, Erber R. A Potential Role of Semaphorin 3A during Orthodontic Tooth Movement. Int J Mol Sci. 2021 Aug 2;22(15):8297. doi: 10.3390/ijms22158297. PMID: 34361063; PMCID: PMC8348452.
原文链接:https://pubmed.ncbi.nlm.nih.gov/34361063/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览以及关注!
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用。
点击了解
细胞流体剪切力|共培养|压力培养|牵张应变|血管培养|平行平板流动腔|仪器|上海泉众机电科技有限公司Naturethink
http://www.Naturethink.com/
Naturethink压力培养|压力刺激|压应力|机械压应力|细胞压力加载|细胞体外加力系统|细胞低压力、细胞正压力|仿生压力细胞培养仪
http://www.Naturethink.com/?product/61.html
联系邮箱:kefu@labbase.net
版权与免责声明
- 凡本网注明“来源:来宝网”的所有作品,版权均属于来宝网,转载请必须注明来宝网, //www.next-search.com,违反者本网将追究相关法律责任。
- 本网转载并注明自其它来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
- 如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。